Phi kim loại (Nonmetal) là một thuật ngữ quen thuộc trong lĩnh vực hóa học, vật lý học. Được sử dụng để chỉ đến các nguyên tố hoặc hợp chất không có tính chất kim loại. So với những nguyên tố và hợp chất kim loại, phi kim loại thường có những đặc điểm và tính chất khác biệt, ảnh hưởng đến cách chúng tương tác với môi trường xung quanh. Trong bài viết này, chúng ta sẽ cùng tìm hiểu về phi kim loại, đặc điểm của chúng, sự khác biệt so với kim loại và ứng dụng của chúng trong đời sống và ngành công nghiệp.
Phi kim loại là gì?
Định nghĩa về phi kim loại
Phi kim loại (Tên

tiếng anh là : Nonmetal) là các nguyên tố và hợp chất không có tính chất kim loại. Chúng thường có đặc điểm tương đối giống nhau, bao gồm các tính chất vật lý và hóa học như không dẫn điện, không dẫn nhiệt, giảm thiểu khả năng dẫn điện khi tăng nhiệt độ, thường có màu sắc tối đa và khả năng hòa tan trong nước tương đối cao. Chúng cũng có thể ở dạng lỏng, dạng rắn hoặc dạng khí tùy loại chúng ta đang xét
Các loại phi kim loại chúng ta thường thấy hiện nay như sau:
- Nguyên tố hiđrô (Hydrogen): Là nguyên tố duy nhất nằm ở cùng bảng với kim loại trong bảng tuần hoàn. Nó thường được tìm thấy ở dạng khí và có nhiều ứng dụng trong công nghiệp, như sản xuất khí đốt, sản xuất động cơ nhiên liệu, v.v.
- Nitơ (Nitrogen): Là một khí rất phổ biến trong khí quyển, và có nhiều ứng dụng trong các ngành công nghiệp như sản xuất phân bón, chất tẩy rửa, chất chống ô nhiễm, v.v.
- Oxy (Oxygen): Cũng là một khí phổ biến trong khí quyển, là một nguyên tố quan trọng cho sự sống của các loài sinh vật, và có nhiều ứng dụng trong y tế, hàn, cắt, nấu ăn, v.v.
- Hợp chất clo (Chlorine compounds): Là nhóm hợp chất chứa nguyên tố clo, được sử dụng trong sản xuất thuốc trừ sâu, chất tẩy rửa, và xử lý nước uống, v.v.
Các ví dụ khác cũng bao gồm nguyên tố khí Helium, khí độc có trong hơi cayenne, hợp chất không ion cacbon (carbon dioxide), và nhóm halogen gồm Fluorin, Clorin, Bromin, và Iodin…
Lịch sử nghiên cứu của phi kim loại qua các thời kỳ

- Thời cổ đại:
- Trong thời kỳ cổ đại, người ta đã nhận ra sự tồn tại của các nguyên tố phi kim loại như cacbon, lưu huỳnh và hiđrô.
- Các nguyên tố này đã được sử dụng trong các quá trình sản xuất và công nghiệp như sản xuất sắt từ quặng sắt.
- Thế kỷ 17 – 18:
- Trong thời kỳ này, nhà hóa học phát triển hệ thống phân loại các nguyên tố và chia chúng thành kim loại và phi kim loại.
- Nguyên tố hidro được phát hiện và được công nhận là một phi kim loại.
- Thế kỷ 19:
- Thời kỳ này chứng kiến sự phát triển đáng kể trong việc tìm hiểu về các loại hợp chất này
- Các nhà khoa học tiếp tục phát hiện ra nhiều nguyên tố phi kim loại mới như nitơ, oxi, lưu huỳnh và phospho.
- Sự hiểu biết về tính chất và ứng dụng của các hợp chất này đã tiến bộ vượt bậc trong lĩnh vực y tế, nông nghiệp, công nghiệp và các lĩnh vực khác.
- Thế kỷ 20 – 21:
- Trong thời kỳ này, nhiều phát hiện quan trọng về phi kim loại đã được thực hiện.
- Các nhà khoa học tiếp tục nghiên cứu và khám phá về cấu trúc, tính chất và ứng dụng của các nguyên tố và hợp chất phi kim loại.
- Công nghệ và ứng dụng của phi kim loại trong lĩnh vực vật liệu, năng lượng, môi trường và y tế đã có những bước tiến đáng kể.
Phi kim loại trong bảng tuần hoàn hóa học
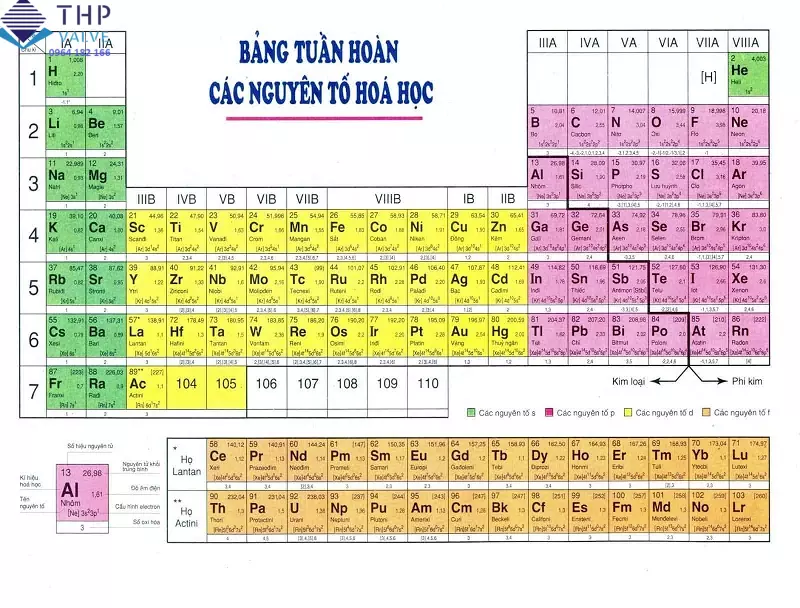
Hiện nay trong bảng tuần hoàn hóa học, các nguyên tố này được phân loại thành các nhóm dựa trên cấu trúc electron của chúng.
Phi kim loại là các nguyên tố nằm ở bên trái của bảng tuần hoàn, bao gồm nhóm 13 đến 18 (trừ nhóm 17) và các nguyên tố trên cùng bên phải của nhóm 11 và 12.
Các nguyên tố có cấu trúc electron phức tạp và ít dẫn điện hơn so với các kim loại. Tính chất vật lý và hóa học của nó thường không đồng nhất và có sự khác biệt lớn với nhau.
Các nguyên tố quan trọng bao gồm bor (B), cacbon (C), nhôm (Al), silic (Si), phốtpho (P), lưu huỳnh (S), selenium (Se), gôm (Ge), arsenic (As), antimon (Sb), tellur (Te), và poloni (Po).
Một số nguyên tố phi kim loại như B, Si, Ge được sử dụng rộng rãi trong các ứng dụng vật liệu, điện tử và pin. Các nguyên tố khác như S, Se, Te có ứng dụng trong lĩnh vực điện tử và y tế.
Các tính chất vật lý và hóa học của các nguyên tố phi kim loại

Tính chất vật lý của phi kim loại
- Đa số các chất này thường có màu sáng và trong suốt.
- Hầu hết các nguyên tố phi kim loại đều là chất rắn, tuy nhiên, có một số nguyên tố như cacbon (C) và lưu huỳnh (S) có thể là chất khí.
- Các nguyên tố phi kim loại có nhiệt độ nóng chảy và nhiệt độ sôi thấp hơn so với các kim loại, nghĩa là chúng dễ chuyển từ trạng thái rắn sang trạng thái khác.
- Nó có khối lượng riêng thấp hơn so với các kim loại, nghĩa là chúng nhẹ hơn và có độ dẻo cao hơn.
- Tính chất dẫn điện và dẫn nhiệt của phi kim loại thường thấp hơn so với các kim loại, nhưng độ bền của chúng thường cao hơn.
- Các nguyên tố này có tính chất hóa học đa dạng và phong phú, chúng có thể tạo thành các hợp chất phức tạp và kết hợp với các nguyên tố khác để tạo ra các hợp chất phong phú và đa dạng.
- Điểm nóng chảy và điểm sôi của các nguyên tố phi kim loại thường rất đa dạng. Chẳng hạn, điểm nóng chảy của bor là 2076°C, trong khi đó điểm nóng chảy của phốtpho là chỉ 44°C.
- Các loại nguyên tố này thường có cấu trúc tinh thể phức tạp, chẳng hạn như cấu trúc tinh thể bản lưới của cacbon đa hình (graphite) và kim cương (diamond).
- Một số nguyên tố phi kim loại, chẳng hạn như lưu huỳnh và selenium, có tính chất nửa dẫn, có thể dẫn điện nhưng không dẫn điện tốt như kim loại hoặc không dẫn điện như chất không dẫn điện.
- Tính chất phản ứng hoá học của các nguyên tố phi kim loại thường có tính chất khó dự đoán do cấu trúc electron phức tạp và sự tương tác giữa các lớp electron khác nhau.
Tính chất hóa học của phi kim loại
- Các nguyên tố phi kim loại thường có độ âm điện cao hơn so với các kim loại, nghĩa là chúng có xu hướng tạo thành các liên kết phân cực và tương tác với các phân tử có độ âm điện cao hơn.
- Các nguyên tố phi kim loại có thể tạo ra nhiều hợp chất hóa học khác nhau. Chẳng hạn, cacbon có khả năng kết hợp với các nguyên tố khác để tạo ra các hợp chất phức tạp như protein, bột đá, sợi cacbon, than đá, và các hợp chất hữu cơ khác.
- Một số nguyên tố phi kim loại, chẳng hạn như lưu huỳnh và selen, có tính chất nửa dẫn, có thể tương tác với kim loại để tạo ra các chất bán dẫn. Ngoài ra hai nguyên tố này cũng có tính chất quang hóa học, có khả năng tương tác với ánh sáng để tạo phản ứng hoặc các hiện tượng quang học
- Các nguyên tố phi kim loại thường có tính chất axit yếu và có thể tương tác với các hợp chất bazơ để tạo ra các muối. Chẳng hạn, phốtpho có khả năng tạo ra các muối phốt phát và adenosin trifosfat (ATP), một hợp chất quan trọng trong quá trình chuyển hóa năng lượng của tế bào.
- Các nguyên tố phi kim loại cũng có thể tương tác với các nguyên tố kim loại để tạo ra các hợp chất hóa học phức tạp. Chẳng hạn, lưu huỳnh có thể tương tác với kim loại như đồng để tạo ra đồng sunfat.
So sánh giữa kim loại và phi kim loại

Đây hoàn toàn là các chất khác nhau các bạn nhé. Để làm rõ vấn đề này chúng tôi xin mời bạn tham khảo bảng so sánh chi tiết của kim loại và phi kim loại để chúng ta có thể nắm được rõ hơn tính chất của hai loại này
| Điểm so sánh/Loại | Kim loại | Phi kim loại |
| Độ âm điện | Thấp hơn phi kim rất nhiều | Có giá trị từ trung bình đến cao |
| Liên kết hóa học | -Ít tạo thành liên kết cộng hóa trị
-Có tính chất tương tác hóa học tốt với các nguyên tố khác, có khả năng hòa tan trong axit và tạo ra muối. -Kim loại có thể tạo thành oxit bazơ khi phản ứng với oxi. |
-Thường xuyên hình thành liên kết cộng hóa trị
-Có tính chất tương tác hóa học kém hơn, nhiều phi kim loại không phản ứng được với axit và không thể tạo muối. -Phi kim có thể tạo thành oxit axit khi phản ứng với oxi |
| Tính chất vật lý | -Tính dẫn điện, dẫn nhiệt tốt.
-Các nguyên tố kim loại có thể tạo thành các ion mang điện tích dương bằng cách mất điện tử của chúng khi phản ứng với một phi kim loại. |
-Không có tính dẫn điện hoặc dẫn điện kém.
-Phi kim có thể tạo thành các ion điện tích bằng cách thu được điện tử của chúng khi phản ứng với kim loại. |
| Điểm nóng chảy | Điểm nóng chảy và độ bền cao | Độ bền cơ học và điểm nóng chảy ở mức thấp |
Ứng dụng của phi kim loại

Các loại phi kim loại hiện nay có ứng dụng vô cùng lớn trong cả công nghiệp và cuộc sống hiện đại. Dưới đây là một số ứng dụng của các loại này trong công nghiệp và cuộc sống hiện nay
- Silicon (Si): Silicon được sử dụng để sản xuất vi mạch, các linh kiện điện tử và các thiết bị điện. Nó cũng được sử dụng để sản xuất pin mặt trời, thuốc nhuộm và các sản phẩm y tế.
- Các hợp chất phi kim loại như silic, germani, arsenic, tellur và selen có tính chất bán dẫn, được sử dụng để sản xuất các thiết bị điện tử như transistor, chip, màn hình điện tử.
- Carbon (C): Carbon được sử dụng để sản xuất đồng hồ và bút chì, nó cũng là thành phần chính trong các sản phẩm như sợi cacbon, các bộ phận tàu vũ trụ, đồ gia dụng, và vật liệu cơ khí. Được phối trộn theo tỉ lệ với các chất ứng dụng rất nhiều trong vật liệu chế tạo hiện nay như các loại thép hình xây dựng, các loại van bằng thép(Van cầu thép, van bi thép, van cổng thép….)
- Sulfur (S): Sulfur được sử dụng để sản xuất lưu huỳnh sulfuric, loại axit mạnh và là thành phần chính của pin và phân bón.
- Phosphorus (P): Phosphorus được sử dụng để sản xuất các sản phẩm hóa học, phân bón, thuốc diệt cỏ, thuốc súc vật và các chất tẩy rửa.
- Boron (B): Boron được sử dụng trong sản xuất bê tông và sợi thủy tinh, cũng như trong sản xuất vật liệu chịu lửa, các sản phẩm điện tử và các sản phẩm y tế.
- Nitrogen (N): Nitrogen được sử dụng làm khí bảo quản thực phẩm, là thành phần của các phân bón và các hợp chất hữu cơ như amino axit.
- Oxygen (O): Oxygen là thành phần chính của không khí, nó cũng được sử dụng trong y tế và chữa cháy.
- Hydrogen (H): Hydrogen được sử dụng để sản xuất khí hydro, làm chất làm lạnh, chất nhiên liệu cho các xe ô tô và máy bay, cũng như trong các sản phẩm hóa chất.
- Ứng dụng trong thời trang và làm đẹp: Kim cương là một trong số các loại trang sức có giá trị cực lớn và được yêu thích nhất
- Một số hợp chất phi kim loại như chất độn (talc, silic) được sử dụng để tăng độ dày và độ nhớt của thực phẩm. Các hợp chất chống bám dính như oxit kẽm và oxit titan cũng được sử dụng trong sản xuất các sản phẩm dùng trong nấu ăn như chảo chống dính.
Trên đây là toàn bộ nội dung bài viết về phi kim loại. Bài viết đã giới thiệu cho bạn đọc hiểu và nắm rõ được khái niệm phi kim loại là gì? Các tính chất của nó(Bao gồm tính chất vật lý và tính chất hóa học)
Ngoài ra chúng tôi cũng đã đưa ra so sánh sự khác nhau giữa kim loại và phi kim loại cho bạn đọc hiểu và nắm được cụ thể. Tầm quan trọng của phi kim loại trong công nghiệp và cuộc sống hàng ngày chúng tôi cũng đã nêu rõ rong phần ứng dụng của nó
Hẹn gặp lại các bạn ở những nội dung sau trong lĩnh vực công nghiệp.

